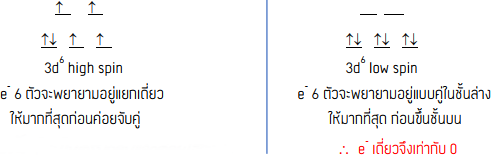Hemoglobin เป็นโปรตีนที่ทำหน้าที่ในการรับและขนส่งแก๊สออกซิเจนมีโครงสร้างที่ประกอบด้วยโปรตีน 4 สาย โดยที่แต่ละสายจะมี active site (บริเวณที่จับแก๊สออกซิเจน) ที่มีโครงสร้างเป็นสารประกอบเชิงซ้อนของ Fe(II) โดยที่ Fe(II) เกิดพันธะกับ N ทั้ง 4 ของ protoporphyrin IX และเกิดพันธะกับ N ของกรดอะมิโน histidine ในรูป deoxy form (ยังไม่จับแก๊สออกซิเจน) Fe(II) จะเป็น Fe(II)-high spin (อิเล็กตรอนใน d-orbital ของโลหะจัดตัวในลักษณะที่มีอิเล็กตรอนเดี่ยวมากที่สุด) แต่หลังจับแก๊สออกซิเจนแล้วจะเกิดการเปลี่ยนแปลงซึ่งยังมีข้อถกเถียงของ Pauling และ Weiss เกี่ยวกับเลขออกซิเตชันของเหล็กและออกซิเจนดังแผนภาพต่อไปนี้
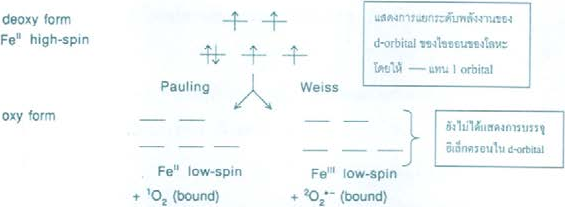
จากข้อมูลข้างต้นจำนวนอิเล็กตรอนเดี่ยวของไอออนของเหล็กใน oxy form (Fe(II) low-spin) ตามแนวความคิดของ Pauling มีค่าเท่าใด(เลขอะตอมของ Fe = 26)
ตอบ ข้อ 1.) 0
เหตุผล
จัดเรียง 26Fe ได้เป็น 1s2 2s2 2p6 3s2 3p6 4s2 3d6
Fe(II) คือ Fe2+ คือ การเสีย e- ชั้นนอกสุด(ชั้น 4s) ออกไป 2 ตัว กลายเป็น 1s2 2s2 2p6 3s2 3p6 4s0 3d6 หมายความว่า d orbital มี e– บรรจุอยู่ 6 e– ซึ่งในกรณี ที่ยังไม่จับกับออกซิเจน (deoxy form) จะเป็นแบบ high spin แต่ถ้าจับกับออกซิเจนแล้ว oxy form จะเป็นแบบ low spin คือ จับเป็นคู่มากกว่า